杨灿王尔华顾小萍马正良
消化内镜已成为消化道疾病诊疗的重要手段,但内镜对咽部、胃肠道的刺激常引起患者不同程度的痛苦,这使得相当一部分患者须在适当地镇静、镇痛下状态才能完成内镜下操作。传统的单纯丙泊酚或以丙泊酚为主的无痛麻醉方案,可使患者处于无意识状态,但对呼吸、循环往往有明显地抑制作用[1]。近一年来,我院将瑞芬太尼复合小剂量丙泊酚的可唤醒无痛麻醉技术应用于消化内镜诊疗中,取得了较满意的效果,现总结报道如下。
一、资料与方法
1. 病例资料:本组自愿接受可唤醒无痛麻醉状态下内镜诊疗患者5334例,男2468例、女2 866例,年龄9 ~ 100 岁,体质量20 ~105 kg,麻醉风险分级(ASA 分级)Ⅰ~Ⅲ级。胃镜检查2635例,胃镜治疗390例;小肠镜检查51例;结肠镜检查2188例,结肠镜治疗70例。
2. 麻醉方法:内镜诊疗前常规胃肠道准备,禁食禁饮6 ~8 h。入室后建立静脉通路,摆好操作体位,常规双鼻式导管吸氧(2 ~4 L/ min)。3 min 内缓慢推注瑞芬太尼40μg + 丙泊酚约30mg(具体用量根据患者病情可适当调整)进行诱导,当患者镇静程度达到Ramsay 分级[2]2 ~ 3 级时开始进镜,内镜操作过程中给予瑞芬太尼约5 μg/ min 静脉维持,患者出现不适时酌情追加丙泊酚10 ~30 mg + 瑞芬太尼10 μg,1 ~2 min 后若患者仍有不适再次追加上述剂量的丙泊酚和瑞芬太尼,直至患者不适体征消失。内镜操作过程中尽量保持患者处于可唤醒状态,如患者血氧饱和度(SpO2 )下降(SpO2 <95%),先唤醒患者嘱其深呼吸,若呼之不应(SpO2<90%)则给予托起下颌处理或面罩辅助呼吸。对于内镜诊疗预估操作时间较长者,术中联用右旋美托咪啶0. 4 ~0. 8 μg·kg--1·min-1持续泵入。
3. 观察项目:监测患者术前、术中、术后平均动脉压(MAP)、心率(HR)、SpO2 ,记录麻醉药物用量、内镜操作时间、不良反应发生情况、术中记忆、患者不适评分及满意度评分。患者不适评分包括术中和术后不适评分两部分,接受胃镜诊疗者术中不适评分由麻醉医师评估,术后不适评分以及接受小肠镜、结肠镜诊疗者术中不适评分由患者进行评估。评分结果分为0 ~4 分,0 分指无不适,4 分指非常不适。患者满意度评分结果分为0 ~ 100 分,0 分指不满意,100 分指非常满意。
4. 统计学分析:采用SPSS 统计软件进行数据分析,计量资料以均数±标准差表示,比较行配对t检验(正态分布者),P <0. 05 为差异有统计学意义。
二、结果
1. 诊疗完成及用药情况:本组均顺利完成内镜下相关诊疗。(1)胃镜检查用时(6. 3±2. 8)min,瑞芬太尼用量(66. 7±19. 8)μg,丙泊酚用量(42. 3±15. 1)mg,未联用右旋美托咪啶;胃镜治疗用时(25. 8 ± 16. 3)min,瑞芬太尼用量(155. 5±71. 5)μg,丙泊酚用量(61. 1 ± 38. 1)mg,右旋美托咪啶用量(23. 2 ± 11. 7)μg。(2)小肠镜检查用时(64. 1±23. 6)min,瑞芬太尼用量(288. 1 ± 108. 1)μg,丙泊酚用量(112. 2±45. 8)mg,右旋美托咪啶用量(37. 0 ± 13. 4)μg。(3)结肠镜检查用时(11. 6±5. 3)min,瑞芬太尼用量(95. 6±33. 0)μg,丙泊酚用量(54. 3±28. 0)mg,未联用右旋美托咪啶;结肠镜治疗用时(27. 0±10. 8)min,瑞芬太尼用量(166. 2 ±68. 1)μg,丙泊酚用量(84. 2 ±104. 5)mg,右旋美托咪啶用量(20. 0 ±0. 0)μg。
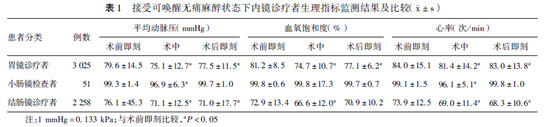
2. 生理指标变化情况:所有患者术中及术后即刻MAP和HR 监测值较术前即刻有不同程度降低,但均在可接受的范围之内(下降幅度<30%);术后即刻SpO2 均恢复至术前即刻水平,接受胃镜、结肠镜诊疗者术中SpO2 下降比较明显,而接受小肠镜检查者术中SpO2 无明显变化。详细结果见表1。
3. 术中记忆发生情况:(1)3 025 例接受胃镜诊疗者中,775 例(25. 62%)存在术中记忆,其中753例为无害记忆(175例追加麻醉药物,578 例未追加),其余22 例(0. 73%)诉有不良记忆(21例追加麻醉药物,1例未追加);2250例诉无术中记忆,其中2 151 例追加麻醉药物,99例未追加。(2)51 例接受小肠镜检查者中,44 例(86. 27%)存在术中记忆,其中42 例为无害记忆(38例追加麻醉药物,4例未追加),其余2例(3. 92%)回忆有轻度腹胀、腹痛(均追加麻醉药物);8 例诉无术中记忆,其中7 例追加麻醉药物,1例未追加。(3)2 258 例接受结肠镜诊疗者中,648 例(28. 70%)存在术中记忆,其中638 例为无害记忆(237 例追加麻醉药物,401 例未追加),其余10例(0. 44%)回忆有轻度腹胀、腹痛(9例追加麻醉药物,1例未追加);1610例诉无术中记忆,其中1 576 例追加麻醉药物,34例未追加。
4. 患者不适评分及满意度评分情况:(1)接受胃镜诊疗者术中不适评分(1. 07± 1. 12)分,术后不适评分(0. 01±0. 11)分,患者检查满意度评分(99. 9 ± 1. 2)分,治疗满意度评分(100. 0 ±0. 0)分;(2)接受小肠镜检查者术中不适评分(1. 93±0. 46)分,术后不适评分(0. 11±0. 45)分,患者检查满意度评分(100. 0±0. 0)分;(3)接受结肠镜诊疗者术中不适评分(1. 93±1. 12)分,术后不适评分(0. 02±0. 15)分,患者检查满意度评分(99. 6±4. 5)分,治疗满意度评分(100. 0±0. 0)分。
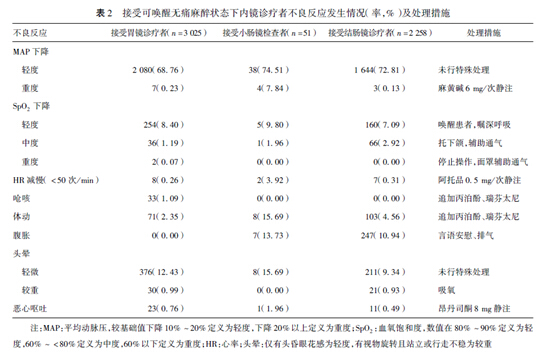
5. 不良反应发生情况:我们将SpO2下降、HR 减慢(<50 次/ min)、MAP 下降视为不良事件,同时观察呛咳、体动、头晕、恶心呕吐等不良反应发生情况,具体发生情况及处理措施详见表2。
讨论
无痛麻醉的目的是使患者术中无明显不适、无不良记忆,操作中患者可控、可满足操作要求,同时术后能快速恢复到术前意识水平[3]。目前,临床上常采用的麻醉药物有丙泊酚、瑞芬太尼等。丙泊酚镇静作用较强,而镇痛作用相对较弱,对呼吸、循环系统抑制作用明显;瑞芬太尼镇痛作用较强,兼有一定的镇静作用,在患者达到相对无痛的同时可以保持一定的清醒状态,但单独使用瑞芬太尼满足麻醉要求所用药量往往较大,有可能出现阿片类药物的副作用,甚至导致痛觉过敏或痛觉异常[4]。术中唤醒技术起先用于脑外科手术术中大脑功能区定位及脊柱侧弯矫形术中评估神经功能[5-6],近一年来我们将瑞芬太尼为主复合小剂量丙泊酚可唤醒无痛麻醉技术应用于消化内镜诊疗中,术中尽量保持患者处于可唤醒、能听从医护人员指令的状态,取得了较好的临床效果。
本组5334例接受胃肠镜诊疗者中,术中及术后即刻MAP 和HR 均较术前即刻有不同程度下降,但均在可以接受的范围之内,仅31 例需要药物进行干预;总体SpO2 无明显改变,绝大部分SpO2 下降者可通过指令或托下颌使SpO2恢复正常,仅1例发生严重紫绀(可能与推药速率较快,发生肌僵直有关),面罩加压辅助通气后恢复正常;有182例(3. 12%)发生体动现象,但仅少数(7例)发生乱动、躁动。
目前,患者对可唤醒无痛麻醉技术的最大顾虑来自于对术中刺激引起的不良记忆的担忧,这些痛苦的阴影也是患者不愿意再次接受此类无痛麻醉技术的主要原因之一。本组5334例接受胃肠镜诊疗者中,术中出现不适者及时追加麻醉药物,最终绝大部分患者转化为无术中记忆或术中仅为无害记忆,仅有34 例(0. 58%)术后诉有不良记忆,且均为患者可接受的腹胀、腹痛,所有患者总体满意度评分接近100 分。既往针对如何优化无痛麻醉方案的研究较多,研究者虽对配伍用药及用药剂量方面进行了大量改进,但几乎都将麻醉深度控制在患者无意识水平。Poulos 等[7]报道胃镜检查单纯应用丙泊酚剂量达(153. 0±59. 2)mg,结肠镜检查单纯应用丙泊酚剂量达(151. 0±92. 7)mg;另有报道称胃镜检查即使伍用瑞芬太尼(0. 5 μg/ kg)后丙泊酚用量仍需达2. 7 mg/ kg[8];至于预估操作时间较长的小肠镜检查,多需要气管插管应用较大量镇静、镇痛和肌松药物维持较深的麻醉
深度[9]。而我们采用的这一可唤醒无痛麻醉技术,虽然所用药物品种较多,但用药平衡,总体用药量较少、花费少,内镜诊疗过程中能保持患者处于可唤醒状态,呼吸抑制时能听从医护人员指令进行深呼吸,在一定程度上能配合医护人员操作,甚至可以主动配合调整体位,诊疗完毕时几乎所有患者能被叫醒,极大地降低了麻醉医师的精神压力,减轻了恢复室的工作压力。
综上所述,瑞芬太尼复合小剂量丙泊酚可唤醒无痛麻醉技术可安全有效地用于消化内镜诊疗。在诊疗过程中患者可保持清醒镇静状态,能够配合操作者调整体位,并且术后无明显不良记忆,总体满意度高,还可节俭医疗资源。
参考文献
[1 ]岳伟,张丽,郭强. 无痛苦胃肠镜技术应用十年分析[J]. 中华消化内镜杂志,2012,30(2):97-99.
[2 ]Ramsay MA,Savege TM,Simpson BR,et al. Controlled sedation with alphaxalone-alphadolone[J]. Br Med J,1974,2(5920):656-659.
[3 ]Ellett ML. A literature review of the safety and efficacy of using propofol for sedation in endoscopy[J]. Gastroenterol Nurs,2010,33(2):111-1117.
[4 ]Lee C,Kim YD,Kim JN. Antihyperalgesic effects of dexmedetomidine on high-dose remifentanil-induced hyperalgesia[J ].Korean J Anesthesiol,2013,64(4):301-307.
[5 ]Bilotta F,Stazi E,Delfini R,et al. Language testing during awake"anesthesia"in a bilingual patient with brain lesion adjacent to Wernicke' s area[J]. Anesth Analg,2011,112(4):938-939.
[6 ]胡丽君,李勇,顾小萍,等. 右旋美托咪定对脊柱侧弯矫形术患者术中唤醒的影响[J]. 国际麻醉学与复苏杂志,2013,34(4):304-307.
[7 ]Poulos JE,Kalogerinis PT,Caudle JN. Propofol compared with combination propofol or midazolam/ fentanyl for endoscopy in a community setting[J]. AANA J,2013,81(1):31-36.
[8 ]Xu ZY,Wang X,__________Si YY,et al. Intravenous remifentanil and propofol for gastroscopy[J]. J Clin Anesth,2008,20(5 ):352-355.
[9 ]Amornyotin S,Kachintorn U,Kongphlay S. Anesthetic management for small bowel enteroscopy in a World Gastroenterology Organization Endoscopy Training Center[J]. World J Gastrointest Endosc,2012,4(5):189-193.
(收稿日期:2014-02-27)
(本文编辑:顾文景)